|
|
Твердое тело и его загадки
Твердое тело и его загадкиКристаллы. Холодное зимнее небо роняет снежинки. Они невесомо опускаются на вашу
ладонь, тают и падают с руки прозрачными шариками — каплями воды. Если
взглянуть на снежинку через лупу, обнаружится сказочное явление: шестилучевая
звездочка, и каждый луч ее состоит из шестигранных столбиков (по-научному —
гексагональных призм). Это кристаллы льда — твердой воды.
Твердое состояние вещества — кристаллическое (см. ст. «Семь состояний материи»). В кристаллах с первого взгляда поражает их правильная форма, у
каждого вещества своя.
Кристаллы поваренной соли (NaCl) образуют кубы. Кристаллы алмаза — октаэдры,
или восьмигранники (см. рис. 1 на цвет. табл. ). Кристаллы
полудрагоценного камня берилла — гексагональные призмы, торцы которых покрыты
тончайшим узором. Не каждый ювелир смог бы воспроизвести такой узор!
Симметрия. Основные внешние признаки твердого тела — его правильная кристаллическая
форма и плоскогранность. Правильность формы выражена в его симметрии, т. е. в
свойстве совмещаться в разных положениях с положением исходным. Если
кубический кристалл повернуть на 90° вокруг оси симметрии, проходящей через центры
противоположных граней, кристалл совместится с исходным положением. При
полном повороте вокруг оси на 360° этот кристалл совместится с исходным положением
четырежды (рис. 1). 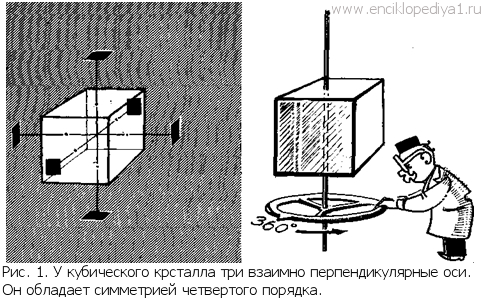 Кристалл NaCl обладает тремя осями симметрии четвертого порядка (они показаны на
рисунке), четырьмя осями третьего порядка (объемные диагонали куба) и шестью
осями второго порядка (они проходят через центры противоположных ребер). Кристалл NaCl обладает тремя осями симметрии четвертого порядка (они показаны на
рисунке), четырьмя осями третьего порядка (объемные диагонали куба) и шестью
осями второго порядка (они проходят через центры противоположных ребер).
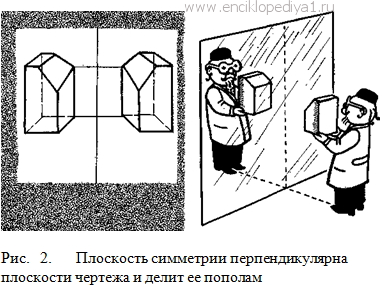
Фигура на рисунке 2, или, например, изображение левой и правой перчаток,
обладают другой, зеркальной симметрией: левая половина рисунка совмещается с
правой, как предмет со своим отражением в зеркале. Вместо оси симметрии здесь
существует плоскость симметрии. На рисунке 2 плоскость симметрии пересекает
плоскость рисунка по линии, делящей рисунок пополам, и обе плоскости
перпендикулярны друг другу. Плоскости симметрии есть и у кристалла (куба) NaCl.
Шаровая форма. Все твердые тела, как бы ни различались они составом и
кристаллической формой, будучи расплавлены, переходят в жидкое состояние и
стремятся тогда принять одну и ту же форму — форму шара, капли. Шаровая форма
типична для жидкости.
Существуют, правда, переохлажденные жидкости, например оконное стекло.
Расплавленная стекольная масса при быстром охлаждении не успевает
закристаллизоваться. Стекло по внешнему виду — твердое тело, а по внутренней
структуре — жидкость. Если его нагреть выше определенной температуры, оно
постепенно, а не сразу, как кристалл, превратится в жидкость.
Монокристаллы и поликристаллические вещества. Твердое тело может быть монокристаллическим,
т. е. состоять из одного-единственного кристалла, или поликристаллическим, т.
е. состоять из многих кристаллов, иной раз очень мелких, например в тысячную
долю миллиметра. В производстве меди или стали расплав охлаждают быстро и
отдельные кристаллики не успевают подрасти. Получается поликристаллическое
твердое тело. Металлические предметы, окружающие нас в быту, от вилки до
подъемного крана, состоят из поликристаллических веществ. Структуру такого вещества можно увидеть через микроскоп.
 Таким образом, поликристаллические вещества состоят из мелких
монокристаллов. Но не следует думать, что монокристаллы всегда мелки. В природе
нередко встречаются крупные монокристаллы. Они вырастают в результате вековых
процессов, протекающих в земной коре. Например, монокристаллы кварца, химический
состав которого тот же, что и у речного песка (SiO2), вырастают
до десятков сантиметров в поперечнике. В Ленинградском горном институте
хранятся монокристаллы кварца, найденные на Урале и на Украине. Высота одного
из них 85 см и вес 800 кг, высота другого 83 см, но он менее широк и весит всего полтонны.
В связи с развитием новой техники появилась потребность, например для
полупроводниковых приборов, как в мелких, так и в крупных монокристаллах
германия, кремния и других веществ. Иногда оказываются нужными кристаллические
иглы, нити и даже тончайшие пленки. Все эти «капризы» приборостроительной
промышленности удовлетворяются научными лабораториями и специальными заводами.
Закон анизотропии. На монокристаллах легко проследить действие одного из
важнейших законов природы, относящихся к твердым телам,— закона анизотропии.
Суть его в том, что многие свойства в твердых телах зависят от направления, в
котором эти свойства измеряются. Например, теплопроводность Кристалла,
измеренная в различных направлениях, может оказаться неодинаковой. Она будет одинаковой лишь в параллельных и
симметричных направлениях. То же можно сказать об электропроводности,
твердости, прочности и других свойствах. Иначе говоря, симметрия внешней формы
сопровождается в кристаллах симметрией физических свойств.
Закон анизотропии проявляется весьма наглядно. Из монокристаллов кварца,
к примеру, изготовляют пьезоэлектрические пластинки (см. ст. «Звук»). Вырезать
их нужно под строго определенными углами к осям симметрии, к граням и ребрам
кристалла и для разных назначений пластинки — под разными углами. Ошибся в
углах среза — получится бракованный прибор.
Симметрия внешней формы и симметрия физических свойств на первый взгляд
кажутся чудом. Они вызваны симметрией внутреннего строения кристалла, т. е.
расположением атомов в твердом теле.
Элементарная ячейка кристаллической решетки. Исследование методами
рентгеновского анализа показало, что правильная форма кристаллов, например
кубическая у NaCl, вызвана правильным расположением в пространстве атомов (точнее, ионов, т.
е. атомов, несущих положительный или отрицательный заряд: Na+ и Сl-). Их расстояния друг от друга строго равны по трем взаимно
перпендикулярным осям.
Наименьшее количество атомов кристалла, сохраняющее при уменьшении его
размеров присущую данному кристаллу симметрию, называется элементарной
ячейкой. На цветной таблице у стр. 376 (рис.2) показана элементарная ячейка
кристалла NaCl. Ребро ее равно 5,63 Е, расстояние между центрами ионов Na+ и Сl- равно 2,815 Е.
Из элементарных ячеек слагается кристаллическая решетка твердого тела,
состоящая из огромного количества атомов. Атомы (ионы) образуют узлы
кристаллической решетки. Промежутки между узлами, «незанятые позиции» называют
междоузлиям. В кристаллической решетке NaCl ионы Na+ и Сl- образуют соответствующие подрешетки натрия и хлора, как бы вставленные
друг в друга. На цветной таблице изображены также элементарные ячейки: меди —
(рис. 3), графита — (рис. 4) и алмаза — (рис. 5). У каждого атома в решетке
меди 12 соседей, в решетке NaCl — 6 соседей, в решетке алмаза — 4. Число
соседей называется координационным числом. Кристаллическую решетку можно
рассматривать как совокупность миллиардов приложенных друг к другу
элементарных ячеек.
Так как в решетке NaCl расстояние между ионами равно 2,815 Е, то вдоль
1 см вещества (ребро куба) уложилось
бы 35,5 млн., или 3,55•107 атомов. Следовательно, в монокристалле
поваренной соли, объем которого равен 1 см3, около 4,45•1022 атомов.
Трудно представить себе такое колоссальное количество! Поясним его таким
примером. Если бы в сосуд было помещено миллион лет назад 4,5•1022
атомов (скажем, гелия) и ежесекундно из этого сосуда вылетал бы в космическое
пространство миллион атомов, то за год количество гелия уменьшалось бы в сосуде
на 3,2•1013 атомов. А за миллион лет оно уменьшилось бы всего на
3,2•1019 атомов, т. е. менее чем на одну тысячную первоначального
количества (4,5•1022).
Структура кристалла и закон анизотропии. Даже в кубической структуре
кристалла типа NaCl, в которой расстояния между атомами одинаковы по трем направлениям, в
других направлениях (кроме этих трех) свойства кристалла сильно отличаются.
Происходит это не только потому, что в других направлениях межатомные
расстояния другие, но и вследствие иного распределения сил связи между атомами.
Возьмем, например, в кристалле NaCl направление объемной диагонали.
Перпендикулярно ей чередуются плоскости, образующие грани октаэдра (см. рис. 2
на цвет. табл.). Каждая из этих плоскостей состоит только из одного типа ионов:
из Na+ или из Сl-. Силы притяжения, возникающие между такими плоскостями, в 5 раз больше,
чем между плоскостями, параллельными граням куба, в каждой из которых лежат и
те и другие ионы: и Na+,
и Сl-. Вот почему кристалл NaCl гораздо легче расколоть по плоскостям куба, чем по плоскостям октаэдра.
Поэтому же и кристаллизуется поваренная соль, образуя кубы. Непонятная на
первый взгляд «прихоть» природы оказывается вполне объяснимой!
У алмаза тоже кубическая решетка. Но атомы углерода предпочитают
образовывать октаэдрические кристаллы. Каждый атом в алмазе окружен четырьмя
соседями (см. рис. 5 на цвет. табл.). Расстояние между ними строго равно 1,54
А. Такие короткие связи очень прочны, недаром алмаз — самое твердое природное
вещество на Земле. Все четыре связи одинаковы, но, если из алмаза вырезать
симметричный куб, количество связей, проходящих через единицу поверхности на
грани такого куба, значительно больше, чем на грани октаэдра. Поэтому-то
алмаз гораздо легче раскалывается (и кристаллизуется) по граням октаэдра, а не по граням куба.
В не кубических кристаллах закон анизотропии проявляется еще более
разительно. На цветной таблице (рис. 4) показана кристаллическая
гексагональная решетка графита. Графит, как и алмаз, состоит из атомов
углерода. Но атомы образуют в нем не октаэдры, а шестиугольные кольца. В
пределах слоя этих колец расстояние между атомами равно всего 1,45 Е. Эти связи
очень прочны, прочнее, чем у алмаза. У каждого атома в слое три связи.
Четвертая же связь, перпендикулярная слою, очень длинна — 3,35 Е — и потому
слаба. Она легко рвется. Графит хорошо расщепляется вдоль слоев решетки и
очень мягок. В направлениях, параллельных и перпендикулярных к слоям, в графите
резко отличаются не только твердость, но и теплопроводность, электропроводность
и многие другие свойства.
Реальные кристаллы. В идеальном кристалле, каким мы только что его описали, «дальний»
порядок охватывает миллионы миллионов атомов. В тех же кристаллах, которые
существуют в природе, т. е. в реальных кристаллах, этот порядок чаще всего
нарушен (см. на цвет. табл. рис. 6). В простом веществе, допустим в меди, атомы
могли бы занять все узлы решетки только при абсолютном нуле, т. е. при 0 °К.
При более высокой температуре атомы переползают из глубины кристалла на его поверхность, оставляя внутри незанятые узлы,
«вакансии». Строение такой решетки называется «структурой Шоттки». При еще
более высокой температуре атомы просто смещаются с узлов в междоузлия —
образуется «структура Френкеля». Атомы примесей могут проникнуть в кристалл и
занять места в свободных узлах. Такое построение называется структурой
замещения. Могут они поместиться и в междоузлиях, тогда возникает структура
внедрения.
В химических соединениях или сплавах их компоненты могут образовывать
между собой структуры замещения. При повышении температуры все больше атомов
одного компонента проникает в позиции второго компонента и, наоборот, атомы
второго компонента — в позиции первого. Беспорядок в кристаллах усиливается.
Все эти нарушения правильной структуры кристаллов в отдельных узлах или
междоузлиях называются точечными
дефектами. Они очень влияют на механические, электрические и другие
свойства кристаллов. Кроме точечных дефектов, в твердых телах и стеклах
возникают и протяженные дефекты,
которые также отражаются на многих свойствах вещества, например на прочности
(трещины, сдвиги слоев и др.).
Механическая прочность тела. Железная проволока сечением в 1 мм2 разрывается силой тяжести в 100 кг. У стеклянной нити того же сечения сопротивление может быть разным; допустим, что оно 10 кг3 (в среднем). Можно ли
считать, что это подлинная прочность стекла? Советские ученые доказали, что
если вместо одной толстой стеклянной нити сечением в 1 мм2 взять стеклянное волокно, допустим, из 1000 нитей с
сечением у каждой в 0, 001 мм2, то прочность такой составной нити будет
уже 100 кг/мм2, т. е. сравняется с прочностью железной
проволоки.
Причина такого загадочного явления оказалась прежде всего в ...
трещинах. Если одна-единственная крохотная трещина возникнет в волокне с
сечением в 1 мм2, то под действием нагрузки эта трещина начнет
быстро удлиняться, пока волокно не лопнет. Если та же трещина возникнет в
одном из волокон нити, состоящей из 1000 тончайших волоконец, то это волокно
также лопнет, но другие 999 волокон останутся неповрежденными и стеклянная нить
выдержит нагрузку.
Это замечательное явление уже используется в технике. Стеклянное волокно,
склеенное пластмассой,— прочный материал «стеклопластик». Из него можно делать
детали машин, не менее прочные, чем из стали, но гораздо более легкие. Многим
любителям рыбной ловли уже известны великолепные удилища из стеклопластика. Они
легки и очень прочны.
Такое свойство реальных кристаллов и стекол открывает перед техникой
практические, очень важные перспективы:
1. Если нужно резко повысить прочность твердого тела, не обязательно
создавать новое вещество. Устранив дефекты, можно во много раз повысить
прочность уже известного вещества. Советские ученые давно доказали такую
возможность.
2. Чтобы понизить прочность твердого тела и тем самым облегчить его помол
(дробление), можно ввести в него так называемые поверхностно-активные вещества,
которые проникают по трещинам в глубь кристалла и значительно облегчают его
раскалывание. Это также доказали своими исследованиями советские ученые — П.
А. Ребиндер и др. (см. ст. «Замечательные явления на границах между телами»).
Удивительные свойства
полупроводников. Много веков известны человечеству
металлы. Из них изготовлялись машины, оружие, утварь. В прошлом веке открыли
возможность передавать на многие тысячи километров электрическую энергию, т,
е. поток электронов. Металлы, например серебро, медь и алюминий, оказались
превосходными проводниками электричества. Электрические провода изготовляются
сейчас из меди и алюминия, а для очень точных приборов — и из серебра.
Для электропередач, кроме проводов, потребовались и изоляторы, например слюда,
фарфор. Такие материалы называют диэлектриками. Они практически не проводят
ток и препятствуют его потерям в электрической сети. Но существует много
веществ, промежуточных по электропроводности между металлами и диэлектриками.
Они и проводники плохие, и изоляторы негодные. Их назвали полупроводниками. До
второй четверти нашего века они не вызывали особый интерес. А сейчас нет
школьника, который не слыхал бы о фантастических свойствах полупроводников
(см. ст. «Полупроводники») .
Полупроводники способны непосредственно превращать энергию нагретых тел и
даже энергию солнечного луча в энергию электрическую. Полупроводники позволяют
сильно уменьшить размеры многих приборов. Например, электронно-счетная машина
совсем еще недавно занимала целый зал. Машина с такими же возможностями,
построенная на полупроводниках, может быть помещена в чемодане.
Мотор-генератор, превращающий переменный ток в постоянный, весит полтонны, а
полупроводниковый выпрямитель тока такой же мощности — всего полкилограмма.
О многочисленных применениях полупроводников подробно рассказано в
статье «Полупроводники». Все эти богатейшие для техники возможности кроются в
крохотных кусочках твердых или стеклообразных тел, обладающих свойствами
полупроводников.
В чем сущность свойств
полупроводника? Почему, например, металл свинец не
может заменить в технике своих соседей по четвертой группе периодической
системы — полупроводники германий и кремний?
Различие между металлами, полупроводниками и диэлектриками вызвано
тонкими деталями в строении атомов и особенностями энергетических уровней в
твердых телах. Атом любого элемента состоит из положительно заряженного ядра и
окружающих ядро электронов. Число электронов в атоме равно порядковому номеру
элемента в периодической системе. Электроны расположены в оболочках, на
уровнях, строго определенных для каждого элемента. Число электронов для
каждого уровня строго ограничено. Между уровнями — «запрещенные» для электронов
области. Электрон может при определенных условиях «соскочить» со своего
уровня, но тогда он должен перейти на соседний уровень. Механизм электронных перескоков в атомах
любых элементов один и тот же: переход с уровня, более близкого к ядру, на
более дальний требует затраты строго определенного количества энергии — кванта
энергии ( + Е); при обратном переходе выделяется такой же квант энергии (-Е).
Когда твердое тело образуется, происходит сближение атомов. Одинаковые
уровни в миллиардах атомов влияют друг на друга, эти уровни чуть-чуть
смещаются, и в твердом теле возникает полоса, или зона уровней. Если самая
внешняя зона заполнена электронами (тогда ее называют валентной), то перемещение
электронов в электрическом поле невозможно, так же как и перемещение пассажиров
в битком набитом трамвае. 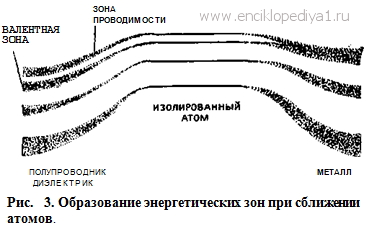 Следовательно, невозможна и электропроводность. Если
же валентная зона перекрыта (рис. 3) зоной, в которой электронов нет или их
мало (зона проводимости), то электроны валентной зоны легко переходят в зону
проводимости и могут там перемещаться в электрическом поле (электронная
проводимость). Электроны, оставшиеся в валентной зоне, приобретают заметную
способность передвигаться в определенном порядке, который называется дырочным
механизмом. Следовательно, невозможна и электропроводность. Если
же валентная зона перекрыта (рис. 3) зоной, в которой электронов нет или их
мало (зона проводимости), то электроны валентной зоны легко переходят в зону
проводимости и могут там перемещаться в электрическом поле (электронная
проводимость). Электроны, оставшиеся в валентной зоне, приобретают заметную
способность передвигаться в определенном порядке, который называется дырочным
механизмом.
Электрические свойства твердого тела зависят от разности энергий валентной
зоны и зоны проводимости. Если зона проводимости и валентная зона взаимно
перекрываются — это металл (см. рис.7 на цвет. табл. ); если зоны не
перекрываются и энергетический разрыв ∆Е (запрещенная зона) между валентной зоной и зоной проводимости невелик —
это полупроводник; если зоны не перекрываются и энергетический разрыв ∆Е велик — это диэлектрик.
Когда валентная зона и зона проводимости не перекрываются, электрон,
чтобы перескочить через запрещенную зону, должен получить квант энергии ∆Е, например, за счет теплового движения
атомов или за счет действия света. В валентной зоне, когда из нее уходит
электрон е-, остается
положительно заряженная «дырка» е+.
В зоне проводимости электроны е-
движутся в электрическом поле к аноду, т. е. к положительному электроду.
Это электронная проводимость. Электроны валентной зоны перескакивают на
свободные места (на положительные «дырки») и также передвигаются к аноду,
оставляя за собой «дырки». Этот процесс удобнее описать так, что «дырки» е+ движутся к отрицательному
электроду — к катоду. Поэтому такой процесс и назван дырочной проводимостью. Сумма обоих процессов —
электронной и дырочной проводимости — определяет электропроводность чистейшего
полупроводника.
Когда температура полупроводника повышается, из валентной зоны все
больше и больше электронов переходит в зону проводимости. В 1 см3 чистейшего германия 4•1022 атомов; при комнатной температуре из валентной зоны переходит в зону
проводимости только 1013 электронов, т. е. 1 электрон на 4•109 атомов. При температуре 300° Ц такой
переход совершают уже 1017 атомов, т. е. в 1000 раз больше. Электропроводность
Ge очень быстро растет при повышении температуры.
Аналогично ведет себя полупроводник, когда на него падает свет, если
энергия светового кванта достаточна для перескока одного электрона.
В обыкновенном дверном звонке электрическая цепь разомкнута. Нажимая
пальцем кнопку, вы соединяете эту цепь, и сигнализация начинает работать. Если
в разрыве цепи поместить не кнопку, а пластинку полупроводника, прибор
становится автоматическим. При комнатной температуре и в темноте сопротивление
в такой цепи очень велико и ток через полупроводник не идет. Но если
полупроводник хотя бы незначительно нагреется (например, когда вблизи возник
пожар), его электропроводность сильно возрастет, и звонок поднимет тревогу.
Можно сконструировать и прибор, который автоматически включит противопожарные
устройства.
Если луч света, падающий на полупроводник, периодически прерывается
проходящими мимо людьми, электропроводность полупроводника то возрастает
(освещение), то падает (тень). И полупроводник будет автоматически включать и
выключать счетчик. Прибор точно сосчитает, сколько людей прошло. Так устроены на многих производствах
автоматические счетчики для регистрации сходящих с конвейера готовых деталей.
Примесная электропроводность. Если полупроводник не чистый и в
нем есть какая-то незначительная
примесь, которую даже невозможно определить обычным химическим анализом,
физики
говорят, что в нем «следы примеси». Свойства полупроводника со следами
примеси
уже иные, чем у чистого. Возьмем, например, полупроводник Ge со следами
As. У атома As 5 внешних электронов (это элемент 5-й группы
периодической системы), а у
тома Ge 4 внешних электрона. Лишний электрон в валентной зоне не нужен,
так как
все места в атомных связях заняты. В таком полупроводнике возникает
около зоны
проводимости «донорный», т. е. отдающий электроны, примесный уровень
(см. рис.
7 на цвет. табл.). Энергетический разрыв ∆ED между зоной
проводимости и примесной зоной очень мал, электрону
примесного уровня нужно придать очень мало энергии, чтобы он мог
перескочить в
зону проводимости. При комнатной температуре каждый атом As отдает в
зону проводимости 1 электрон. Допустим, что в этом
полупроводнике 1 атом As приходится на 108 атомов Ge. Следовательно, в 1 см3 на 4•1022 атомов 4•1014
атомов As. Уже при комнатной температуре в зоне проводимости окажется 4•1014 электронов, т. е. в 40 раз больше, чем в
беспримесном полупроводнике. Полупроводник с донорным примесным уровнем называется
электронным и обозначается буквой n, например n-Ge.
Следы примеси галлия придают германию уже совсем другие свойства. В
валентной оболочке галлия всего 3 электрона. Следовательно, в каждой
связи не
хватает одного электрона в результате замены атома Ge на атом Ga. В
валентной зоне такого полупроводника образуются положительные дырки,
а в запрещенной зоне появляется акцепторный, т. е. принимающий
электроны,
уровень. Перескок электрона из валентной зоны на акцепторный уровень
также
требует ничтожную затрату энергии. Он происходит уже при комнатной
температуре.
Такой примесный полупроводник называется дырочными обозначается буквой р, например p-Ge, Примесь 1 атома галлия на 108 атомов германия вызывает высокую
дырочную электропроводность.
Ученые и инженеры, комбинируя электронные и дырочные полупроводники,
создают многочисленные «чудодейственные» приборы.
Загадка термоэлектрогенератора. Если привести в соприкосновение электронный и дырочный полупроводники
и нагреть место их соединения, то на холодном конце электронного полупроводника
сгруппируются электроны е-, а
на холодном конце дырочного полупроводника — дырки е+. Такая пара полупроводников называется
термоэлектрогенератором. Соединив холодные концы полупроводников проводом, можно
получить ток. Это легко обнаружить, нагрев место соединения полупроводников и
включив электролампочку в цепь.
Полупроводниковый выпрямитель тока. Если ввести в полупроводник различные примеси, можно получить в нем
области — электронную и дырочную. В таком полупроводнике образуется
пограничный слой между этими областями. Пограничный слой иногда называют p-n-переходом. Он позволяет использовать полупроводник
как выпрямитель тока. Когда к дырочной области (+области) подключен анод ( +
электрод), а к электронной области (-области) подключен катод (-электрод), то
ток, естественно, легко проходит через полупроводник (пропускное направление).
Но если к +области подключить -электрод, а к -области подключить +электрод, то
заряды оттекут от p-n-перехода к противоположно заряженным электродам и ток через полупроводник почти не
сможет проходить (запорное направление). Движение электронов и положительных
дырок через цепь регулируется p-n-переходом с огромной скоростью
В одном и том же полупроводнике можно поместить два и более p-n-переходов. Это позволяет создавать
транзисторы. Такие транзисторы — основная действующая часть крохотных
радиоприемников, легких переносных телевизоров и других замечательных
приборов. Главная загадка примесных
полупроводников. Свойства твердых тел определяются их
химическим составом и строением элементарных ячеек. Но за последние десятилетия
выяснилось, что закон постоянства состава («где бы и как бы соединение ни
получалось, его состав и свойства всегда одни и те же») для твердых тел иногда
неприменим. Например, в сульфиде свинца PbS на атом Pb не
обязательно приходится один атом S, а формулу сульфида свинца правильнее
было бы понимать как соотношение Pb и S между Pb 0,9995 S и PbS 0,9995. Если тело — полупроводник, как в данном
случае, то даже ничтожные отклонения индексов РЬ и S в сторону недостатка серы или свинца
влекут за собой резкие изменения электропроводности и других физических
свойств (иногда в миллионы раз!). Меняется и знак проводимости. Недостаток
серы ведет к образованию электронного, а недостаток свинца — дырочного
сульфида свинца. Мы столкнулись здесь с неожиданным и важным явлением: в
основном составе полупроводника не только присутствующие, но и отсутствующие
атомы влияют на его полупроводниковые свойства так же сильно, как и ничтожные
следы примесей. Этот загадочнейший на первый взгляд факт вызван тем, что в
твердом теле разнородные атомы частично ионизированы, т. е. несут на себе тот
или иной заряд: например, Pbn+ Sn-. Если из решетки
кристалла испарить даже следы свинца, то +заряд, который был на этих атомах,
останется в кристаллах, например на вакансии, оставленной испарившимся атомом.
Эти +заряды, условно связанные с вакансиями, совершенно аналогичны акцепторному
дырочному уровню и резко увеличивают электропроводность. Если испарить следы
серы, то - заряды останутся на вакансиях серы и будут вести себя аналогично
электронному донорному уровню, электропроводность также резко возрастет. В
полупроводниках ничтожные концентрации точечных дефектов, вызванные структурой
вычитания, т. е. нехваткой части атомов (см. рис. 6 на цвет. табл.), влекут за
собой исключительно важные научные выводы и технические возможности.
* * *
Мы коснулись здесь только некоторых из многочисленных загадок твердого
тела, которые уже раскрыты пытливым умом исследователей. На пороге знаний —
новые загадки и новые открытия.
Образование есть то, что остается,
когда все выученное уже забыто.
* * *
Луи Пастер: «Не всякому помогает
случай. Судьба одаривает только подготовленные умы» .
* * *
Математические методы исследования часто открывали
перед физиками неожиданные горизонты. Напомним фразу великого французского математика
Анри Пуанкаре: «Уравнения стали умнее тех, кто их выводит».
|
|