|
Меню сайта
|
На пути к искусственному созданию жизниНа пути к искусственному созданию жизниВ искусстве мало ценятся художники, весь талант которых заключается в умении подражать чужим, хотя и действительно прекрасным образцам. Искусство создавать что-то совершенно новое несравненно ценнее и почетнее, чем искусство копировать и подражать. ...Мы давно перестали видеть что-то особенно замечательное в том, что многие продукты лаборатории тождественны с теми или другими произведениями природы. Скорее мы склонны увлечься идеей создания веществ, которых в природе нет и не может быть. Но в одной области искусство человека отстало от искусства природы. Здесь мы еще остаемся подражателями и учениками. Химик может искусственно создавать важнейшие разновидности жиров и углеводов. Он проник в строение белковых веществ, из которых состоит мозг, мускулы, кожные покровы — весь организм людей, животных и других живых существ, вплоть до микробов и вирусов. Простейшие, подобные белкам вещества давно воспроизведены в лаборатории. Практическое значение открытий в этой области науки, казалось бы, должно быть особенно ценным для пищевой промышленности. Умение создавать основные пищевые вещества, исходя, если нужно, из элементов, могло бы перевернуть все дело питания. Но природа поставляет нам белки, жиры и углеводы за несравненно более дешевую цену. Живые организмы — сложнейшие «фабрики», которые возникли и усовершенствовались не в один или два года, а создавались миллионы лет. Белки входят в состав нашего организма в виде массивных
молекул с громадными молекулярными весами, примерно от десяти тысяч и до
нескольких миллионов единиц. В нашем теле содержатся тысячи различных белков,
каждый из которых имеет свое особое строение и выполняет свою особую роль в
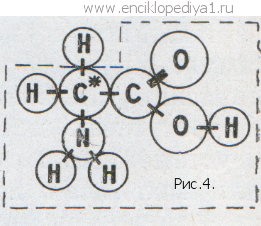
жизнедеятельности организма. При кипячении со щелочами и кислотами громадные молекулы белков расщепляются на мелкие молекулы аминокислот — так плохо скованные цепи распадаются на отдельные звенья. Аминокислоты и являются теми звеньями, из которых слагаются молекулы всех белков. На рисунке 4 представлена структура молекулы простейшей из аминокислот, так называемого глицина. В рамки заключена та группировка атомов, которая сохраняется во всех белковых аминокислотах. Остальные из числа важнейших природных аминокислот, на которые расщепляются природные белки, отличаются от этой лишь тем, что один водородный атом замещен той или другой несложной группой атомов. Это замещение имеет замечательное последствие: отмеченный звездочкой атом углерода становится асимметрическим, т. е. появляется возможность существования молекулы в двух вариантах — «левом» и «правом». Но особенно поразительно другое. Каков бы ни был источник природной аминокислоты — любой растительный или животный вид, любой вид бактерий, молекулы всех природных аминокислот оказываются «левыми»; «правые» аминокислоты в живой природе обнаружены лишь в антибиотиках. То, что происходит с белками в химической колбе,
происходит и в природной «колбе» — в желудке: белки расщепляются в нем на аминокислоты.
Маленькие молекулы аминокислот легко проникают через стенки желудка в кровь и
разносятся по тканям организма, где вновь сцепляются в молекулы белков. Значит,
нам не обязательно питаться белками, можно питаться и непосредственно
аминокислотами? Не обязательно даже, чтобы белковая пища попадала в желудок,
можно впрыскивать раствор аминокислот прямо в кровь? Именно так и поступают
врачи, когда больной страдает настолько глубоким расстройством пищеварения,
что его желудок отказывается переваривать белковую пищу.
Не обязательно также, чтобы в аминокислотной диете содержались все природные аминокислоты. Мы нуждаемся лишь в 9 из них, остальные наш организм может готовить сам. Низшие же организмы способны вырабатывать для себя все необходимые аминокислоты из неорганических веществ. Белковая пища полноценна, когда в ней содержатся все 9 необходимых аминокислот. Таков творог. Если в белковой пище недостает тех или иных аминокислот, она неполноценна. Например, в желатине (белке), образующемся при вываривании костей, недостает трех из числа необходимых человеку аминокислот. Сцепление молекул аминокислот в цепочкообразные молекулы белка осуществляется в тканях нашего организма путем отщепления воды: 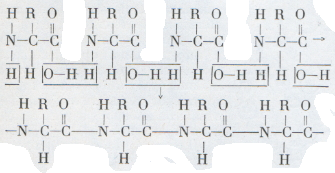 В одних случаях молекулы образующегося белка напоминают нить, свернутую в клубок (такие молекулы образует, например, белок куриного яйца). В других случаях они сохраняют вытянутую форму (такая молекула напоминает длинную пружинку — рис. 5). Из молекул-пружинок, скрученных друг с другом, как проволочки в кабеле или тросе (рис. 6), слагаются волосы, ногти, мускулы и другие волокнистые ткани нашего организма. Эти молекулы действительно обладают свойством пружины: они могут растягиваться до длины, вдвое превышающей их нормальную, и сжимаются вновь, как только растягивающая сила перестает действовать. 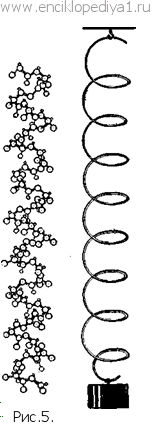 Химик вводит расщепленный белок в прибор-автомат и спустя сутки без своего дальнейшего участия получает готовый результат анализа — график, запечатленный на ленте. Он узнает, какие именно аминокислоты и в каком количественном соотношении входили в состав данного белка. Но далее встает сложная задача — превратить данные анализа в структурную формулу. 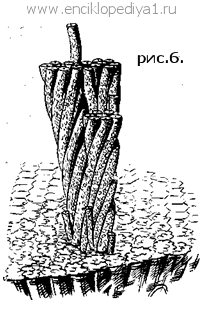 До конца удалось решить ее (с помощью физики и
математики—рентгеновского анализа и электронно-счетных машин) для нескольких
белков, в том числе для одного из животных белков-гормонов — инсулина.
Молекула этого белка состоит из 51 звена, представленного 15 аминокислотами.
Его структурная формула едва уместилась бы на странице этого тома. И вот что
замечательно: последовательность сцепления аминокислотных звеньев строго одна
и та же в инсулине, извлеченном из столь различных животных, как свинья и кит. До конца удалось решить ее (с помощью физики и
математики—рентгеновского анализа и электронно-счетных машин) для нескольких
белков, в том числе для одного из животных белков-гормонов — инсулина.
Молекула этого белка состоит из 51 звена, представленного 15 аминокислотами.
Его структурная формула едва уместилась бы на странице этого тома. И вот что
замечательно: последовательность сцепления аминокислотных звеньев строго одна
и та же в инсулине, извлеченном из столь различных животных, как свинья и кит.
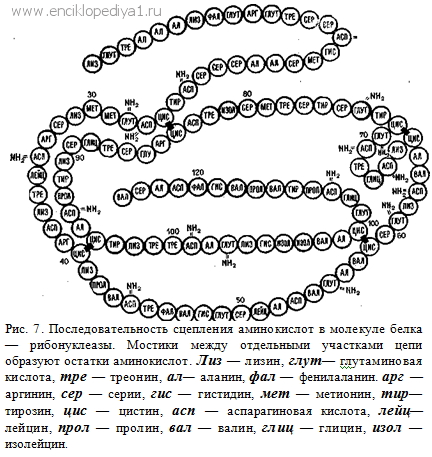
Строение молекул инсулина всех свиней и всех китов повторяется и в инсулине лошади, только в нем в одном из звеньев аминокислота серии заменена глицином; у быка замещены другими аминокислотами два аминокислотных звена, у овцы — три... Это единство плана построения молекулы белка, выполняющего одно и то же назначение в организме разных животных, тем более поразительно, что из 15 аминокислот теоретически можно образовать миллиарды миллиардов (больше, чем, например, волос на головах всех жителей Земли) 51-звенных цепей различного строения, беря одинаковые или различные звенья и смыкая их друг с другом в разном порядке. На рисунке 7 представлена последовательность сцепления аминокислот в молекуле еще более сложного белка — рибонуклеазы; аминокислоты обозначены здесь начальными буквами их названий: сер — серин, вал — валин и т. д. Проблема искусственного белка продолжает штурмоваться в разных направлениях. Но и сейчас химия далека от решения задачи получения белков заводским путем. Таким образом, нельзя особенно надеяться на коренное преобразование в ближайшем будущем современных способов питания. Успехи в искусственном воспроизведении природных белков в какой-то мере приближают нас к решению величайшей теоретической и практической задачи — искусственному созданию жизни. При искусственном воспроизведении белков не обошлось без разочарований. Многие рассчитывали, что создать белок — это и значит создать жизнь. Однако выделено большое количество белков, все они прекрасно сохраняются в пробирках, многие — в виде превосходных кристаллов, но признаков жизни вне живого организма в них так же мало, как в сахаре или крахмале. Это нисколько не поколебало уверенность, что уяснить и осуществить переход от «неживого» к «живому» — цель, доступная именно химическому исследованию. Химик обращается к биологу с вопросом: какими свойствами
нужно наделить молекулу, чтобы она стала «жить»? Тогда уже дело химика думать,
какие сочетания атомов для появления этих свойств следует создать. Многие полагают, что жизнь имеет нехимическое начало, что она началась не с молекулы, а с какого-то уже достаточно сложного сочетания молекул, так как всякий живой организм обладает не только определенным химическим составом, но и определенной организацией. Подробное обсуждение этих мнений будет иметь смысл лишь тогда, когда мы точно определим, что именно разумеем под словом «жить». Для того чтобы решить, что рассматриваемый объект именно живое существо, мы должны установить у него одновременное наличие ряда свойств. Вопрос и заключается в том, можно ли все эти свойства сочетать в одной молекуле. Создавая краски, химик именно так и сочетает в одной молекуле свойство быть окрашенной, свойство сцепляться с волокном и т. д. Ставя таким образом задачу искусственного создания жизни, мы не рассчитываем, как алхимики, что из химической колбы выскочит готовый гомункулус — маленький живой человечек. Ведь живые существа, помимо всего прочего, имеют за собой миллионы лет истории, управляемой законами естественного отбора, и мы вряд ли сможем перепрыгнуть через эту великую пропасть времени. Мы можем рассчитывать лишь создать нечто такое, что, будучи предоставлено самому себе, при благоприятных условиях превратилось бы спустя миллионы лет в растения, животные или нечто подобное тем и другим. Будет ли это искусственно созданное «нечто» веществом
или каким-то сверхпростым организмом? В течение многих лет пристальное
внимание ученых приковано к миру живых существ, недоступных даже сильнейшим
микроскопам. Таков бактериофаг — «пожиратель бактерий». Действие бактериофага
впервые описал русский ученый Н. Ф. Гамалея еще в 1898 г. Это такой же паразит
по отношению к бактериям, как бактерия по отношению к человеку. Бактериофаги
присутствуют всюду, где присутствуют бактерии: в животных организмах, в воде
рек, озер, морей и т. д. Они выделены и из продуктов, не зараженных
бактериями: из чеснока, лука, яблок, моркови. Бактериофагам во всем, кроме условий существования, подобны вирусы — ультрамикроскопические возбудители заразных болезней, таких, как грипп, полиомиелит, бешенство. Первый вирус — возбудитель чумы у рогатого скота — был открыт тем же русским ученым Гамалея за два года до открытия им первого бактериофага. Частицы одних вирусов выглядят в электронном микроскопе, как шарики, других — как тонкие и длинные палочки. По отношению к людям, животным и растениям вирусы ведут себя, как микробы. Живые организмы в свою очередь относятся к ним, как к микробам: в борьбе с вирусами они вырабатывают в себе «антитела», гибельные для данного вида вируса, и в таких случаях, перенеся болезнь, приобретают иммунитет к нему, т. е. повторно этому заболеванию не подвергаются. Естественно, что врачи обращаются с вирусами так же, как с микробами. А химики обращаются с теми же вирусами, как с самыми обыкновенными веществами: они растворяют их, адсорбируют, осаждают и кристаллизуют. |
ПОИСК
Block title
|
 Бактериофаги удалось наблюдать
лишь с помощью ультрамикроскопа и электронного микроскопа. Это инструменты
такой мощной разрешающей силы, что им уже доступны наиболее крупные молекулы.
Итак, бактериофаги имеют размеры массивных молекул! Это материя, раздробленная
на молекулы. Но эта материя живет, т. е. питается и размножается, сохраняя
свои прирожденные свойства. Вокруг бактериофагов разгорелся страстный спор. По
мнению одних, бактериофаг — это вещество, по мнению других — живое существо. Не
есть ли он и то и другое одновременно, думали третьи.
Бактериофаги удалось наблюдать
лишь с помощью ультрамикроскопа и электронного микроскопа. Это инструменты
такой мощной разрешающей силы, что им уже доступны наиболее крупные молекулы.
Итак, бактериофаги имеют размеры массивных молекул! Это материя, раздробленная
на молекулы. Но эта материя живет, т. е. питается и размножается, сохраняя
свои прирожденные свойства. Вокруг бактериофагов разгорелся страстный спор. По
мнению одних, бактериофаг — это вещество, по мнению других — живое существо. Не
есть ли он и то и другое одновременно, думали третьи.