|
Меню сайта
|
Что такое неметаллыЧто такое неметаллыВсе химические свойства элементов связаны с наружными электронными оболочками их атомов (одной или двумя). Наиболее устойчивыми бывают такие оболочки, которые состоят из восьми (неон, аргон и другие инертные газы) или из двух (гелий) электронов. Сравнительно устойчивым является также «ансамбль» из восемнадцати электронов. Движущей силой химической реакции, в которой участвуют элементы, служит стремление каждого из них к созданию устойчивого наружного слоя. Сделать это элемент может двумя способами: или отдать один или несколько электронов, чтобы оставшиеся электроны образовали, например, желанную «восьмерку», или взять недостающее число чужих электронов, «достроить» наружный слой до такого же устойчивого «ансамбля». Посмотрим, как построены атомы некоторых элементов (рис. 1).
Сравнивая для каждого элемента обе эти тенденции, ученые называют неметаллами элементы электроотрицательные, т. е. такие, которые легче принимают электроны, чем отдают их. Когда во внешней электронной оболочке содержится уже много электронов (это относится к элементам V, VI и VII групп периодической системы), у атома должна быть сильнее тенденция брать электроны. Именно поэтому неметаллы занимают правую часть периодической системы. Но если наружная электронная оболочка находится на большом расстоянии от положительно заряженного ядра, то ядро удерживает последние электроны слабо, они теряются легче, а значит, растут металлические свойства элементов. Поэтому в одной и той же группе, идя сверху вниз, мы встречаем все менее электроотрицательные элементы. Углерод и свинец — оба находятся в IV группе, оба содержат по 4 электрона в наружном слое, но радиус атома углерода невелик, ядро прочно удерживает электроны: углерод — неметалл. А свинец — металл, потому что из-за большого расстояния наружной электронной оболочки от ядра электроны последнего слоя легко освобождаются. Легкость, с какой освобождаются наружные электроны, делает металлы хорошими проводниками электричества и тепла. Ведь электрический ток, текущий в металле, и есть поток таких «свободных» электронов. Граница между неметаллами и металлами проходит не по вертикали — это результат совместного действия на электроотрицательность элемента двух факторов: размеров атома и количества электронов в последнем слое. По этой же причине переход от металлов к неметаллам происходит постепенно, нерезко. |
ПОИСК
Block title
|
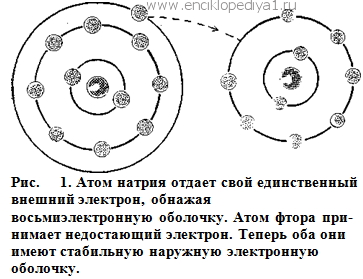 Натрий — типичный металл, потому что для его атома (чтобы наружная оболочка стала восьмиэлектронной) достаточно отдать один электрон; этот путь самый легкий, самый выгодный. А для фтора решение достигается по-другому: взяв еще один электрон, фтор достроит свою наружную электронную оболочку до восьмиэлектронной. Для атома хлора возможны оба варианта — взять еще один электрон или отдать семь. Но все-таки первая тенденция сильнее, первый путь более выгодный.
Натрий — типичный металл, потому что для его атома (чтобы наружная оболочка стала восьмиэлектронной) достаточно отдать один электрон; этот путь самый легкий, самый выгодный. А для фтора решение достигается по-другому: взяв еще один электрон, фтор достроит свою наружную электронную оболочку до восьмиэлектронной. Для атома хлора возможны оба варианта — взять еще один электрон или отдать семь. Но все-таки первая тенденция сильнее, первый путь более выгодный. 