|
Меню сайта
|
Электрохимия и учение об электричествеЭлектрохимия и учение об электричествеПроблемой непосредственного превращения химической энергии в электрическую и электрической в химическую занимается электрохимия. Эта наука зародилась в самом начале XIX в. В наши дни она переживает свою вторую молодость.
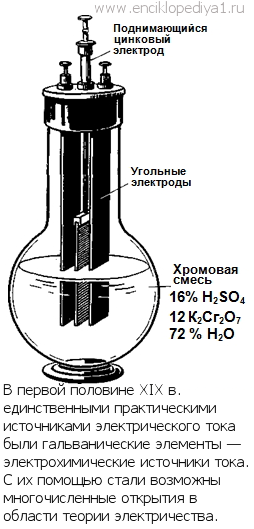
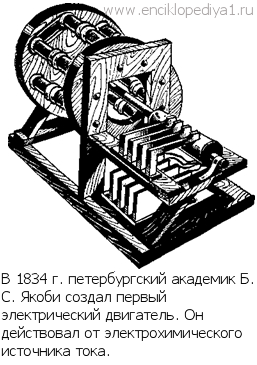
Электрохимические реакции отличаются от обычных химических реакций тем, что в них участвуют свободные электроны. В ходе такой реакции свободные электроны либо выделяются, либо поглощаются. Примерами первых реакций могут служить реакции растворения металлов: Zn→Zn+2+2е или реакции выделения кислорода на положительном электроде при электролизе воды: 4ОН-→2Н2O+O2 +4е. Реакции с отдачей электронов окислительные (металлический цинк, отдавая электроны, окисляется до двухвалентного состояния). В качестве примера вторых, восстановительных реакций назовем реакции отложения металлов из растворов, например Cu+2 +2e→Cu, или реакцию электролитического выделения водорода: 2Н++2е→Н2. Электрохимические реакции протекают на поверхности металлических электродов, погруженных в раствор электролита. Электроны в обычных условиях не могут существовать в водном растворе в свободном состоянии; поэтому их и подводят к реагирующим веществам или отводят от них по электроду. Электрохимические реакции играют большую роль в технике. В течение почти всей первой половины XIX в. единственными источниками электрического тока, которые помогали совершать многочисленные открытия в области теории электричества, были электрохимические источники тока, или гальванические элементы (см. ст. «Электромагнитное поле»). Без этих источников невозможно себе представить ни развития представлений об электромагнетизме, ни создания основ электротехники, ни даже появления первых электромагнитных двигателей и генераторов. Зарождение электроэнергетики неразрывно связано с электрохимическими источниками тока и электрохимическими реакциями, с превращением химической энергии в электрическую. |
ПОИСК
Block title
|